“居家自测”试行在即,这些公司抗原检测产品引关注

金色光投资有道
线索主要标的
大家都在看:
中美谈完了,中方立场!俄乌大消息,泽连斯基发生“紧急情况”!普京怒斥乌军袭击平民,欧盟宣布新制裁!
随着《新冠病毒抗原检测应用方案(试行)》的印发,我国疫情防治或将进入居家自测新阶段,多家公司新冠病毒抗原检测产品获批上市。A股市场上,不少公司披露,积极推进旗下抗原检测产品的注册申请工作。
新冠病毒抗原检测方案试行,10家公司检测产品获批上市
2022年3月11日,国家卫健委发布消息,国务院应对新型冠状病毒肺炎疫情联防联控机制综合组决定在核酸检测基础上,增加抗原检测作为补充,并组织制定了《新冠病毒抗原检测应用方案(试行)》。
该试行方案规定了新冠抗原检测产品适用人群包括:到基层医疗卫生机构就诊,伴有呼吸道、发热等症状且出现症状5天以内的人员;隔离观察人员,包括居家隔离观察密接和次密接、入境隔离观察、封控区和管控区内的人员;以及有抗原自我检测需求的社区居民三类。其中提出,社区居民有自我检测需求的,可通过零售药店、网络销售平台等渠道,自行购买抗原检测试剂进行自测。
而为切实保障新冠病毒抗原检测试剂产品质量安全,进一步强化产品质量安全监管,3月12日,国家药监局综合司发布《关于做好新冠病毒抗原检测试剂质量安全监管工作的通知》(以下简称:《通知》),提出加强注册相关管理工作、加强生产环节监督检查、加强经营环节监督检查、严厉打击违法违规行为四方面工作要求。
《通知》要求,地方各级药品监督管理部门要进一步做好对新冠病毒抗原检测试剂经营企业的监督检查,监督指导企业从具备合法资质的医疗器械注册人、生产经营企业购进新冠病毒抗原检测试剂,做好进货查验和销售等记录,配备相适应的设施设备,保证产品运输、储存条件符合标签和说明书的标示要求。要求重点关注企业经营的新冠病毒抗原检测试剂是否经注册批准并具备合格证明文件,产品说明书是否载明消费者个人自行使用说明等。此外,对从事网络销售的医疗器械经营企业,还要督促其在网站主页面显著位置展示医疗器械经营许可证,在产品页面展示医疗器械注册证等信息。
2022年3月13日,国家药品监督管理局(以下简称:国家药监局)批准了北京万泰生物药业股份有限公司、北京热景生物技术股份有限公司、天津博奥赛斯生物科技股份有限公司、重庆明道捷测生物科技有限公司和北京乐普诊断科技股份有限公司5家新冠抗原检测产品的证明文件(准产)。
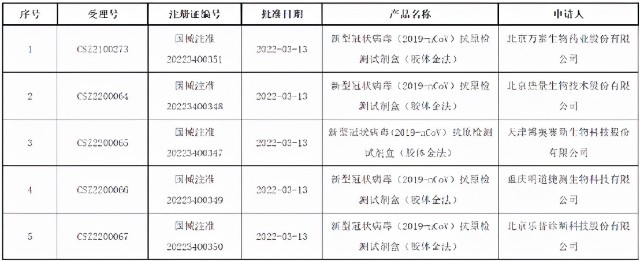

来源:国家药品监督管理局网站
此外,2022年3月11日、3月12日,经国家药品监督管理局批准,南京诺唯赞医疗科技有限公司、北京金沃夫生物工程科技有限公司、深圳华大因源医药科技有限公司、广州万孚生物技术股份有限公司、北京华科泰生物技术股份有限公司的新冠抗原检测产品的证明文件(变更)。至此,我国现阶段共有10款新冠抗原检测产品获批上市。


来源:国家药品监督管理局网站
多家公司披露产品获批上市,股价走高
A股市场上,前述多家公司近日先后披露新冠抗原检测产品获得国家药监局注册批准等相关公告。不过,这些公司均表示,受多重因素影响,目前尚无法预测相关产品对公司未来业绩的影响。
万泰生物(603392.SH)3月14日公告披露, 其公司自主研发生产的新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)近日收到国家药监局颁发的《中华人民共和国医疗器械注册证(体外诊断试剂)》,该产品包装规格为10人份/盒,50人份/盒,用于体外定性检测口咽拭子、鼻咽拭子、鼻拭子样本中新型冠状病毒(2019-nCoV)N抗原。
万泰生物披露,公司的新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)2021年相继获得德国BfArM认证、法国ANSM认证、欧盟CE认证和澳大利亚TGA认证,可在欧盟国家和澳大利亚用于非专业人员自检或专业人员使用。本次在国内获批上市,将有利于提升公司在相关领域的竞争力,对公司的销售和国内业务拓展具有积极作用。其表示,上述产品的实际销量受多重因素影响,产品的后续市场销售情况及利润贡献具有不确定性。
乐普医疗(300003.SZ)3月14日披露,公司控股子公司北京乐普诊断科技股份有限公司研制的新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)于2022年3月13日获得国家药品监督管理局的注册批准,取得III类医疗器械注册证,该产品用于体外定性检测鼻拭子样本中新型冠状病毒(2019-nCoV)N抗原。乐普医疗披露,上述产品的获批有利于进一步拓宽公司产品线,产品实际销售情况受多种因素影响,公司尚无法预测该产品对未来业绩的具体影响。
热景生物(688068.SH)也于3月14日披露,公司自主研发生产的新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)近日收到国家药监局颁发的《医疗器械注册证》,该产品用于体外定性检测鼻拭子样本中新型冠状病毒(2019-nCoV)N 抗原。
诺唯赞(688105.SH)则于3月12日披露,全资子公司南京诺唯赞医疗科技有限公司自主研发生产的新型冠状病毒抗原检测试剂盒近日收到国家药监局颁发的《医疗器械注册证》。公司称,尚无法预测该产品的获批对未来业绩的具体影响。
万孚生物(300482.SZ)3月14日公告披露,公司新型冠状病毒抗原检测试剂盒批准证明文件变更。其新型冠状病毒抗原检测试剂盒(胶体金法)用于体外定性检测口咽拭子、鼻咽拭子、鼻拭子样本中新型冠状病毒N抗原,增加了鼻拭子样本的采样方式。
华大基因(300676.SZ)3月14日公告披露,控股子公司深圳华大因源医药科技有限公司近日取得国家药监局颁发的《中华人民共和国医疗器械注册变更文件(体外诊断试剂)》,对新冠抗原检测产品的医疗器械注册证进行了变更。该产品用于体外定性检测新型冠状病毒感染肺炎疑似人群口咽拭子、鼻咽拭子样本中新型冠状病毒N抗原检测。公司目前尚无法预测其对公司未来业绩的影响。
二级市场上来看,3月14日收盘,上述多股上涨。其中,诺唯赞股价报120.74元/股,涨幅达13.59%;华大基因涨9.98%,股价报98.32元/股;热景生物涨幅为4.31%,股价报200.49元/股。万孚生物、乐普医疗分别上涨3.71%和2.86%。
多家公司提交注册申请
除了上述公司以外,还有多家公司也发布了与新冠抗原检测试剂相关的消息。
明德生物(002932.SZ)股票交易价格于2022年3月9日、3月10日、3月11日收盘价格涨幅偏离值累计超过20%。3月14日,明德生物分别于深交所互动平台及股票交易异常波动公告中披露,公司新冠抗原检测试剂已向国家药品监督管理局提交注册申请,该注册证的取得时间尚存不确定性。
3月14日,九强生物(00406.SZ)在深交所互动易平台回复相关提问时表示,新冠自测版的抗原卡审批需要遵循严格的流程,公司正在积极推进国内及美国新冠抗原检测注册证的申请,未来公司也将密切跟踪国内外体外诊断试剂行业的最新变化,积极拓展海外销售。
此外,谱尼测试(300887.SZ)也在深交所互动易平台上称,公司已经研发出新冠抗原检测试剂,正在准备向国家药品监督管理局提交注册申请,该注册证的取得时间尚存不确定性。其披露,目前公司于北京、深圳、黑龙江、郑州、长春、厦门、武汉、青岛、苏州、天津、大连、上海、内蒙古和西安等地已有14个实验室获批新型冠状病毒核酸检测业务。
来源:金色光投资有道
展开阅读全文
文章观点仅代表作者观点,或基于大数据智能生产,不构成投资建议。投资者依据此做出的投资决策需自担风险,与通联数据无关。